እያንዳንዱ ሰው በህይወቱ ውስጥ ከሦስቱ አጠቃላይ የቁስ ግዛቶች ውስጥ ካሉ አካላት ያጋጥማል። ለማጥናት በጣም ቀላሉ የመደመር ሁኔታ ጋዝ ነው. በአንቀጹ ውስጥ ተስማሚ ጋዝ ጽንሰ-ሀሳብን እንመለከታለን, የስርዓቱን ሁኔታ እኩልነት እንሰጣለን, እና ለፍጹማዊ የሙቀት መጠን መግለጫም የተወሰነ ትኩረት እንሰጣለን.
የጉዳይ ጋዝ ሁኔታ
እያንዳንዱ ተማሪ "ጋዝ" የሚለውን ቃል ሲሰማ ስለ ምን ሁኔታ እንደሚያወራ ጥሩ ሀሳብ አለው። ይህ ቃል ለእሱ የቀረበለትን ማንኛውንም መጠን መያዝ የሚችል አካል እንደሆነ ተረድቷል። ቅርጹን ማቆየት አይችልም, ምክንያቱም ትንሽ የውጭ ተጽእኖን እንኳን መቋቋም አይችልም. እንዲሁም ጋዝ መጠኑን አይይዝም, ይህም ከጠጣር ብቻ ሳይሆን ከፈሳሾችም ይለያል.
እንደ ፈሳሽ ጋዝም ፈሳሽ ነገር ነው። በጋዞች ውስጥ ጠንካራ አካላትን በማንቀሳቀስ ሂደት ውስጥ, የኋለኛው ደግሞ ይህንን እንቅስቃሴ ያደናቅፋል. የተገኘው ኃይል ተቃውሞ ይባላል. ዋጋው በእሱ ላይ የተመሰረተ ነውበጋዝ ውስጥ ያለው የሰውነት ፍጥነት።
የጋዞች ጠንከር ያሉ ምሳሌዎች አየር፣የተፈጥሮ ጋዝ ለቤት ማሞቂያ እና ለማብሰያነት የሚውል፣የማይነቃነቁ ጋዞች (ኔ፣አር) የማስታወቂያ ግሎው ቱቦዎችን ለመሙላት ጥቅም ላይ የሚውሉት ወይም በሚገጣጠምበት ጊዜ የማይነቃነቅ (ጥቃት የሌለበት፣ መከላከያ) አካባቢ ለመፍጠር ይጠቅማሉ።.
ጥሩ ጋዝ
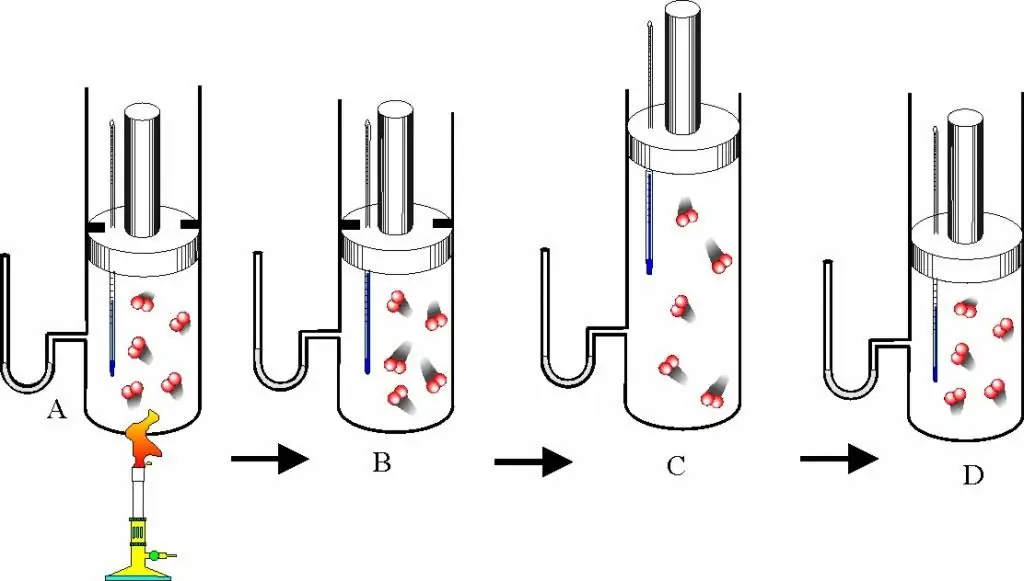
ወደ ጋዝ ህጎች መግለጫ እና የግዛት እኩልነት ከመቀጠልዎ በፊት ጥሩ ጋዝ ምን እንደሆነ የሚለውን ጥያቄ በደንብ መረዳት አለብዎት። ይህ ጽንሰ-ሐሳብ በሞለኪውላር ኪነቲክ ቲዎሪ (MKT) ውስጥ ቀርቧል. ጥሩ ጋዝ የሚከተሉትን ባህሪያት የሚያረካ ማንኛውም ጋዝ ነው፡
- የተፈጠሩት ቅንጣቶች ከቀጥታ ሜካኒካዊ ግጭቶች በስተቀር አይገናኙም።
- ቅንጣቶች ከመርከቧ ግድግዳዎች ጋር ወይም በራሳቸው መካከል በሚፈጠሩ ግጭቶች ምክንያት የእንቅስቃሴ ጉልበታቸው እና ፍጥነታቸው ተጠብቆ ይቆያል ፣ ማለትም ፣ ግጭቱ ፍጹም የመለጠጥ ነው ተብሎ ይታሰባል።
- አንቀጾች ምንም አይነት ልኬቶች የላቸውም፣ነገር ግን የተወሰነ መጠን አላቸው፣ይህም ከቁሳዊ ነጥቦች ጋር ተመሳሳይ ናቸው።
ማንኛውም ጋዝ ተስማሚ አለመሆኑ ግን እውነተኛ ነው። ቢሆንም, ብዙ ተግባራዊ ችግሮችን ለመፍታት, እነዚህ approximations በጣም ትክክለኛ ናቸው እና ጥቅም ላይ ሊውል ይችላል. የሚለው አጠቃላይ ተጨባጭ ህግ አለ፡- የኬሚካል ተፈጥሮ ምንም ይሁን ምን ጋዝ ከክፍል ሙቀት በላይ የሙቀት መጠን ካለው እና የከባቢ አየር ቅደም ተከተል ወይም ዝቅተኛ ግፊት ካለው ከፍተኛ ትክክለኛነት ጋር ጥሩ ተደርጎ ሊወሰድ ይችላል እና ለመግለፅ ሊያገለግል ይችላል። ነው።የግዛቱ ሃሳባዊ የጋዝ እኩልታ ቀመር።
ክላፔይሮን-ሜንዴሌቭ ህግ
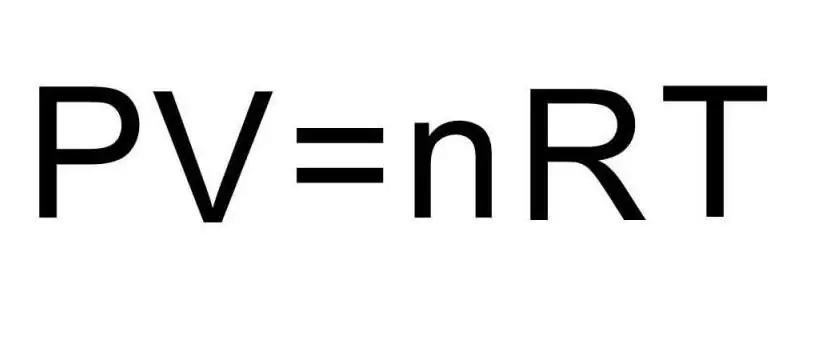
የተለያዩ የቁስ አካላት እና ሂደቶች በአንድ ድምር ሁኔታ መካከል ያሉ ሽግግሮች የሚከናወኑት በቴርሞዳይናሚክስ ነው። ግፊት፣ ሙቀት እና መጠን የቴርሞዳይናሚክስ ስርዓት ማንኛውንም ሁኔታ በልዩ ሁኔታ የሚገልጹ ሶስት መጠኖች ናቸው። የአንድ ሃሳባዊ ጋዝ ሁኔታ እኩልነት ቀመር ሦስቱንም መጠኖች ወደ አንድ እኩልነት ያጣምራል። ይህን ቀመር እንፃፍ፡
PV=nRT
እዚህ P፣ V፣ T - ግፊት፣ መጠን፣ ሙቀት፣ በቅደም ተከተል። የ n ዋጋ በሞለስ ውስጥ ያለው ንጥረ ነገር መጠን ነው, እና ምልክቱ R የጋዞችን ሁለንተናዊ ቋሚ ያመለክታል. ይህ እኩልነት የሚያሳየው የግፊት እና የመጠን ምርት በጨመረ መጠን የቁስ መጠን እና የሙቀት መጠን መሆን አለበት።

የጋዝ እኩልታ ቀመር የክላፔሮን-ሜንዴሌቭ ህግ ይባላል። እ.ኤ.አ. በ 1834 ፈረንሳዊው ሳይንቲስት ኤሚል ክላፔይሮን የቀድሞዎቹን የሙከራ ውጤቶችን ጠቅለል አድርጎ ወደዚህ እኩልነት መጣ። ይሁን እንጂ ክላፔይሮን ብዙ ቋሚዎችን ተጠቀመ, በኋላ ላይ ሜንዴሌቭ በአንድ - ሁለንተናዊ ጋዝ ቋሚ R (8, 314 J / (molK)) ተክቷል. ስለዚህ በዘመናዊ ፊዚክስ ይህ እኩልታ የተሰየመው በፈረንሣይ እና ሩሲያ ሳይንቲስቶች ስም ነው።

ሌላ የእኩልነት ቅጾች
ከላይ፣ የሜንዴሌቭ-ክላፔይሮን ግዛት እኩልነት ለሀገር ጋዝ በአጠቃላይ ተቀባይነት ባለው እና ፅፈናል።ምቹ ቅጽ. ነገር ግን በቴርሞዳይናሚክስ ውስጥ ባሉ ችግሮች ውስጥ ትንሽ ለየት ያለ መልክ ብዙ ጊዜ ሊያስፈልግ ይችላል። ሶስት ተጨማሪ ቀመሮች ከዚህ በታች ተጽፈዋል፣ እነሱም ከተጻፈው እኩልታ በቀጥታ ይከተላሉ፡
PV=NkBT፤
PV=m/MRT፤
P=ρRT/M.
እነዚህ ሶስት እኩልታዎች እንዲሁ ለሀሳባዊ ጋዝ ሁለንተናዊ ናቸው፣ በነሱ ውስጥ ብቻ እንደ mass m፣ molar mass M፣ density ρ እና የስርአቱን የያዙት ቅንጣቶች N ብዛት ይታያሉ። kB እዚህ ያለው ምልክት የቦልትማን ቋሚን (1፣ 3810-23J/K) ያመለክታል።
ቦይሌ-ማሪዮቴ ህግ
ክላፔይሮን እኩልታውን ሲያወጣ ከበርካታ አስርት ዓመታት በፊት በሙከራ በተገኙ የጋዝ ህጎች ላይ የተመሰረተ ነው። ከነዚህም አንዱ የቦይል-ማሪዮት ህግ ነው። እሱ በተዘጋ ስርዓት ውስጥ የኢሶተርማል ሂደትን ያንፀባርቃል ፣ በዚህ ምክንያት እንደ ግፊት እና የድምፅ ለውጥ ያሉ ማክሮስኮፕ መለኪያዎች። T እና n ቋሚን በስቴት እኩልታ ውስጥ ለአንድ ሃሳባዊ ጋዝ ካስቀመጥነው፣ ከዚያም የጋዝ ህጉ የሚከተለውን ቅጽ ይወስዳል፡
P1V1=P2V 2
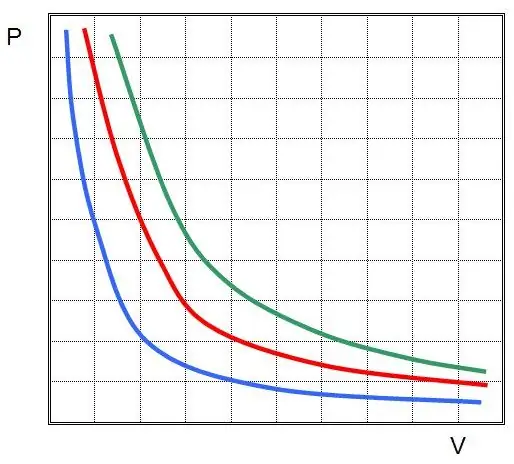
ይህ የቦይል-ማሪዮት ህግ ነው፣የግፊት እና የመጠን ምርት በዘፈቀደ የኢተርማል ሂደት ውስጥ እንደሚጠበቅ ይናገራል። በዚህ አጋጣሚ፣ እሴቶቹ P እና V ራሳቸው ይለወጣሉ።
P(V) ወይም V(P(P) ካሴሩ፣ ኢሶተርሞች ሃይፐርቦላዎች ይሆናሉ።
የቻርለስ እና የጌይ-ሉሳክ ህጎች
እነዚህ ህጎች አይዞባሪክ እና ኢሶኮሪክን በሂሳብ ይገልፃሉ።ሂደቶች, ማለትም በጋዝ ስርዓቱ ግዛቶች መካከል እንዲህ ያሉ ሽግግሮች, ግፊት እና መጠን በቅደም ተከተል ይጠበቃሉ. የቻርለስ ህግ በሂሳብ እንደሚከተለው ሊፃፍ ይችላል፡
V/T=const when n, P=const.
የጌይ-ሉሳክ ህግ እንደሚከተለው ተጽፏል፡
P/T=const when n, V=const.
ሁለቱም እኩልታዎች በግራፍ መልክ ከቀረቡ፣ ከዚያም ወደ x-ዘንጉ በተወሰነ አቅጣጫ ዘንበል ያሉ ቀጥታ መስመሮችን እናገኛለን። ይህ ዓይነቱ ግራፍ በቋሚ ግፊት እና በሙቀት መጠን መካከል ባለው የድምፅ እና የሙቀት መጠን እና በቋሚ መጠን መካከል ባለው ግፊት እና የሙቀት መጠን መካከል ቀጥተኛ ተመጣጣኝነትን ያሳያል።
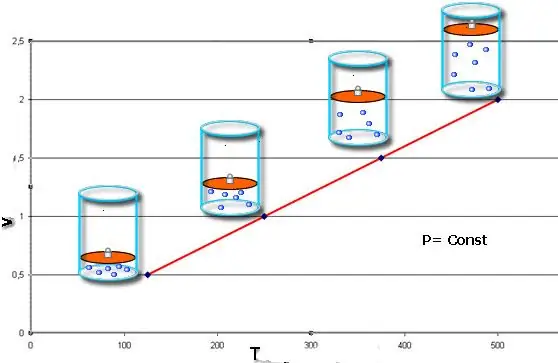
ልብ ይበሉ ሦስቱም የጋዝ ሕጎች የጋዙን ኬሚካላዊ ስብጥር እና የቁሱ መጠን ለውጥን ከግምት ውስጥ ያላስገቡ መሆናቸውን ልብ ይበሉ።
ፍፁም ሙቀት
በዕለት ተዕለት ሕይወት ውስጥ፣ በዙሪያችን ያሉትን ሂደቶች ለመግለፅ ስለሚመች የሴልሺየስ የሙቀት ምጣኔን እንጠቀማለን። ስለዚህ ውሃ በ100 oC ይፈላ እና በ0 oC ላይ ይቀዘቅዛል። በፊዚክስ ውስጥ, ይህ ሚዛን የማይመች ሆኖ ተገኝቷል, ስለዚህ, በ 19 ኛው ክፍለ ዘመን አጋማሽ ላይ በሎርድ ኬልቪን የተዋወቀው ፍፁም የሙቀት መለኪያ ተብሎ የሚጠራው ጥቅም ላይ ይውላል. በዚህ ሚዛን መሰረት፣ የሙቀት መጠኑ የሚለካው በኬልቪን (ኬ) ነው።
በ -273, 15 oC የሙቀት መጠን የአተሞች እና ሞለኪውሎች የሙቀት ንዝረት እንደሌለ ይታመናል፣የፊት እንቅስቃሴያቸው ሙሉ በሙሉ ይቆማል። ይህ በዲግሪ ሴልሺየስ ውስጥ ያለው የሙቀት መጠን በኬልቪን (0 ኪ) ውስጥ ካለው ፍፁም ዜሮ ጋር ይዛመዳል። ከዚህ ትርጉምየፍፁም ሙቀት አካላዊ ትርጉሙ እንደሚከተለው ነው፡- ቁስን የሚፈጥሩት የንጥረ ነገሮች የእንቅስቃሴ ሃይል መለኪያ ነው ለምሳሌ አተሞች ወይም ሞለኪውሎች።
ከላይ ካለው የፍፁም የሙቀት መጠን አካላዊ ትርጉም በተጨማሪ ይህንን መጠን ለመረዳት ሌሎች አካሄዶችም አሉ። ከመካከላቸው አንዱ የተጠቀሰው የቻርለስ ጋዝ ህግ ነው. በሚከተለው ቅጽ እንጽፈው፡
V1/T1=V2/T 2=>
V1/V2=ቲ1/T 2.
የመጨረሻው እኩልነት በሲስተሙ ውስጥ ባለው የተወሰነ መጠን (ለምሳሌ 1 ሞል) እና የተወሰነ ግፊት (ለምሳሌ 1 ፓ) የጋዝ መጠን ፍፁም የሙቀት መጠንን በልዩ ሁኔታ ይወስናል ይላል። በሌላ አነጋገር በእነዚህ ሁኔታዎች ውስጥ የጋዝ መጠን መጨመር የሚቻለው በሙቀት መጨመር ምክንያት ብቻ ነው, እና የድምጽ መጠን መቀነስ የ T.
ዋጋ መቀነስ ያሳያል.
አስታውስ ከሴልሺየስ የሙቀት መጠን በተለየ ፍፁም የሙቀት መጠን አሉታዊ ሊሆን አይችልም።
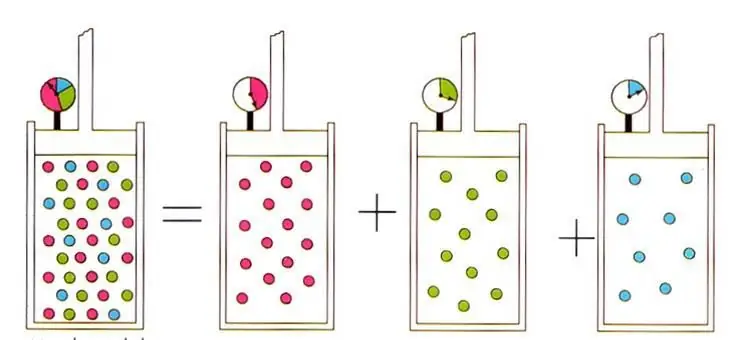
የአቮጋድሮ መርህ እና የጋዝ ቅይጥ
ከላይ ከተጠቀሱት የጋዝ ህጎች በተጨማሪ የግዛት እኩልነት ለሀሳባዊ ጋዝ በ19ኛው ክፍለ ዘመን መጀመሪያ ላይ በአሜዴኦ አቮጋድሮ የተገኘውን መርህም ይመራዋል፣ እሱም የመጨረሻ ስሙን ይይዛል። ይህ መርህ በቋሚ ግፊት እና የሙቀት መጠን ውስጥ የማንኛውም ጋዝ መጠን በሲስተሙ ውስጥ ባለው ንጥረ ነገር መጠን እንደሚወሰን ያረጋግጣል። ተዛማጁ ቀመር ይህን ይመስላል፡
n/V=const ጊዜ P፣ T=const።
የጽሑፍ አገላለጽ ወደ ታዋቂው የጋዝ ፊዚክስ የዳልተን ጋዝ ድብልቅ ህግ ይመራል። ይህሕጉ በድብልቅ ውስጥ ያለው የጋዝ ከፊል ግፊት በልዩ ሁኔታ የሚወሰነው በአቶሚክ ክፍልፋይ እንደሆነ ይገልጻል።
የችግር አፈታት ምሳሌ
የተዘጋ መርከብ ውስጥ ጠንካራ ግድግዳዎች ጥሩ ጋዝ በያዙ ፣በሙቀት ምክንያት ግፊቱ በ 3 እጥፍ ጨምሯል። የስርዓቱ የመጀመሪያ እሴቱ 25 oC.
ከሆነ የስርዓቱን የመጨረሻ የሙቀት መጠን ማወቅ ያስፈልጋል።
በመጀመሪያ የሙቀት መጠኑን ከዲግሪ ሴልሺየስ ወደ ኬልቪን እንለውጥ፡-
አለን።
T=25 + 273፣ 15=298፣ 15 K.
የመርከቧ ግድግዳዎች ጥብቅ ስለሆኑ የማሞቅ ሂደቱ እንደ isochoric ሊቆጠር ይችላል. ለዚህ ጉዳይ፣ የጌይ-ሉሳክ ህግን እንተገብራለን፣ አለን፡
P1/T1=P2/T 2=>
T2=P2/P1T 1.
በመሆኑም የመጨረሻው የሙቀት መጠን የሚወሰነው ከግፊት ጥምርታ ምርት እና ከመጀመሪያው የሙቀት መጠን ነው። መረጃውን ወደ እኩልነት በመተካት መልሱን እናገኛለን፡ T2=894.45 K. ይህ የሙቀት መጠን ከ621.3 oC.
ጋር ይዛመዳል።






