ጋዞች፣ ከቴርሞዳይናሚክስ አንፃር፣ በማክሮስኮፒክ ባህሪያት ስብስብ ይገለፃሉ፣ ዋና ዋናዎቹ የሙቀት፣ ግፊት እና መጠን ናቸው። ከእነዚህ መመዘኛዎች ውስጥ የአንዱ ቋሚነት እና የሁለቱም ለውጥ አንድ ወይም ሌላ isoprocess በጋዝ ውስጥ እንደሚከሰት ያመለክታል. ይህን ጽሑፍ ለጥያቄዎች ዝርዝር መልስ እንሰጣለን - ይህ ischoric ሂደት ነው ፣ በጋዝ ስርዓት ግዛቶች ውስጥ ከ isothermal እና isobaric ለውጦች እንዴት እንደሚለይ።
በፊዚክስ ጥሩ ጋዝ

ይህ የኢሶኮሪክ ሂደት ነው ለሚለው ጥያቄ መልስ ከመስጠትዎ በፊት የፍጆታ ጋዝ ጽንሰ-ሀሳብን በደንብ ማወቅ አለብዎት። በፊዚክስ ውስጥ፣ እንደ ማንኛውም ጋዝ ተረድቷል ፣ በውስጡ ያሉት ንጥረ ነገሮች አማካኝ የእንቅስቃሴ ኃይል በግንኙነታቸው ከሚፈቀደው ኃይል እጅግ የላቀ ፣ እና በእነዚህ ቅንጣቶች መካከል ያለው ርቀት ከመስመራዊ ልኬታቸው የበለጠ በርካታ የክብደት ቅደም ተከተሎች ናቸው። በተጠቀሱት ሁኔታዎች ውስጥ, በሚፈፀምበት ጊዜ, ይቻላልስሌቶች በንጥሎች መካከል ያለውን የመስተጋብር ኃይል ግምት ውስጥ አያስገባም (ከዜሮ ጋር እኩል ነው) ፣ እና እንዲሁም ቅንጣቶች የተወሰነ የጅምላ መጠን ያላቸው የቁሳቁስ ነጥቦች እንደሆኑ መገመት ይቻላል።
በሀሳቡ ጋዝ ውስጥ የሚከናወነው ብቸኛው ሂደት የመርከቧን ንጥረ ነገር ከያዘው የመርከቧ ግድግዳዎች ጋር ቅንጣቶች መጋጨት ነው። እነዚህ ግጭቶች በጋዝ P. ውስጥ የተወሰነ ግፊት መኖሩን በተግባር ያሳያሉ.
እንደ ደንቡ ማንኛውም ጋዝ ያለው ንጥረ ነገር በአንጻራዊ ኬሚካላዊ የማይነቃቁ ሞለኪውሎችን ያቀፈ እና ዝቅተኛ ግፊት እና ከፍተኛ የሙቀት መጠን ያለው ለተግባራዊ ስሌት በቂ ትክክለኛነት ያለው ጥሩ ጋዝ ተደርጎ ሊወሰድ ይችላል።
ተስማሚ ጋዝ የሚገልጽ ቀመር
እርግጥ ነው እየተነጋገርን ያለነው ስለ ክላፔይሮን-ሜንዴሌቭ ዓለም አቀፋዊ ህግ ነው፣ይህም የኢሶኮሪክ ሂደት መሆኑን ለመረዳት በሚገባ መረዳት አለበት። ስለዚህ፣ የመንግስት ሁለንተናዊ እኩልታ የሚከተለው ቅጽ አለው፡
PV=nRT.
ይህም የግፊት P እና የጋዝ መጠን V የፍፁም የሙቀት መጠን T ምርት እና በሞለስ n ውስጥ ካለው ንጥረ ነገር መጠን ጋር እኩል ነው ፣ R የተመጣጠነ ሁኔታ ነው። ሒሳቡ ራሱ ለመጀመሪያ ጊዜ የተፃፈው በኤሚል ክላፔሮን በ 1834 ነው ፣ እና በ 19 ኛው ክፍለ ዘመን በ 70 ዎቹ ዓመታት ዲ ሜንዴሌቭ የአንድ ሁለንተናዊ የጋዝ ቋሚ R (8.314 J / (molK) ቋሚ እሴቶችን ተክቷል።))
በ Clapeyron-Mendeleev እኩልታ መሰረት በተዘጋ ስርዓት ውስጥ የጋዝ ቅንጣቶች ቁጥር ቋሚ ነው, ስለዚህ ሊለወጡ የሚችሉት ሶስት ማክሮስኮፒክ መለኪያዎች ብቻ ናቸው (T, P).እና ቪ) የኋለኛው እውነታ ከዚህ በታች የሚብራሩትን የተለያዩ isoprocesses ግንዛቤን መሰረት ያደረገ ነው።
የአይሶኮሪክ ሂደት ምንድነው?
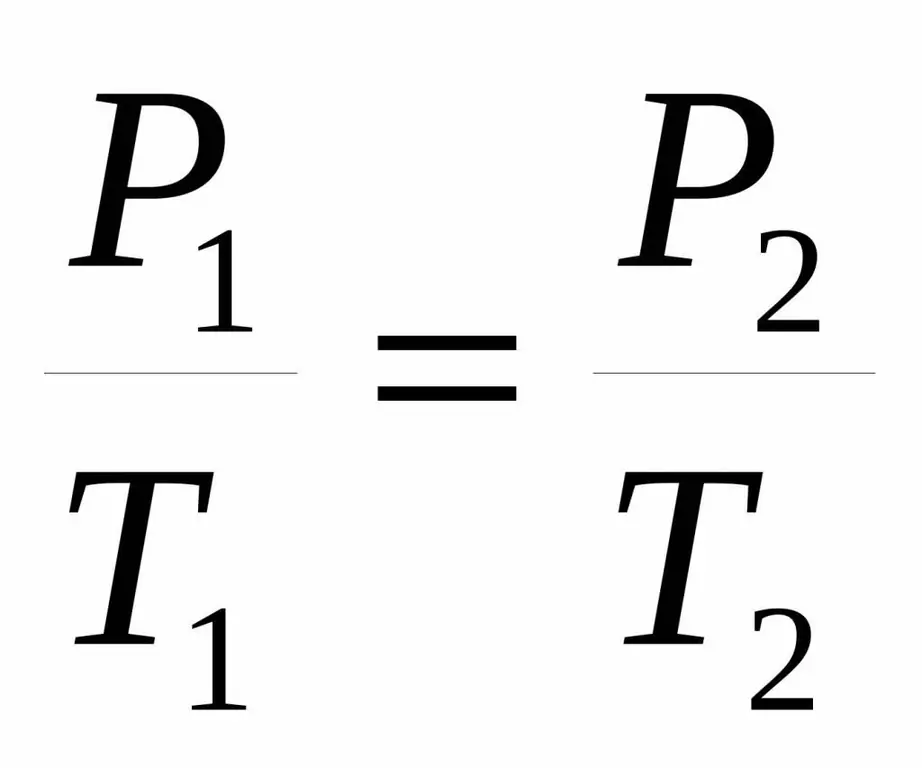
ይህ ሂደት በስርአቱ ሁኔታ ላይ የሚፈጠር ማንኛውም ለውጥ እንደሆነ ተረድቷል፣ይህም መጠኑ የተጠበቀ ነው።
ወደ ዓለም አቀፋዊ የግዛት እኩልታ ከተሸጋገርን፣ በኢሶኮሪክ ሂደት ውስጥ ግፊት እና ፍፁም የሙቀት ለውጥ በጋዝ ውስጥ ብቻ ነው ማለት እንችላለን። የቴርሞዳይናሚክስ መለኪያዎች በትክክል እንዴት እንደሚለወጡ ለመረዳት፣ተዛማጁን የሂሳብ አገላለጽ እንጽፋለን፡
P / T=const.
አንዳንድ ጊዜ ይህ እኩልነት በትንሹ ለየት ባለ መልኩ ይሰጣል፡
P1 / ቲ1=P2 / ቲ 2.
ሁለቱም እኩልነት በ18ኛው ክፍለ ዘመን መገባደጃ ላይ በሙከራ የታወቀው ጥገኝነት ባገኘው ፈረንሳዊ ሳይንቲስት ስም የቻርለስ ህግ ይባላሉ።

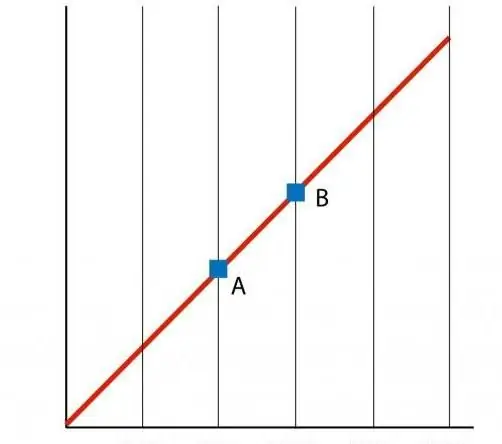
የተግባርን P(T) ግራፍ ከገነባን ቀጥታ መስመር ጥገኝነት እናገኛለን፣ እሱም ኢሶኮሬ ይባላል። ማንኛውም isochore (ለሁሉም የ n እና V እሴቶች) ቀጥተኛ መስመር ነው።
የሂደቱ የኃይል መግለጫ
እንደተገለፀው የኢሶኮሪክ ሂደት በተዘጋ ነገር ግን ያልተገለለ ስርዓት ውስጥ የሚካሄድ የስርዓት ሁኔታ ለውጥ ነው። እየተነጋገርን ያለነው በጋዝ እና በአካባቢው መካከል የሙቀት ልውውጥ ሊኖር ስለሚችል ነው. በአጠቃላይ ማንኛውም የሙቀት Q ወደ ስርዓቱ አቅርቦት ወደ ሁለት ውጤቶች ይመራል፡
- የውስጥ ሃይል ይለውጣል U፤
- ጋዝይሰራል፣ እየሰፋ ወይም እየዋለ ነው።
የመጨረሻው ማጠቃለያ በሒሳብ እንደሚከተለው ተጽፏል፡
Q=U + A.
የሀሳባዊ ጋዝ አይሶኮሪክ ሂደት፣በ ትርጉሙ፣ መጠኑ ሳይለወጥ ስለሚቆይ በጋዝ የሚሰራ ስራን አያመለክትም። ይህ ማለት ለስርአቱ የሚሰጠው ሙቀት ሁሉ የውስጥ ሃይሉን ለመጨመር ይሄዳል፡
Q=U.
በዚህ አገላለጽ ግልጽ የሆነውን የውስጣዊ ሃይል ቀመር ከተተካ የኢሶኮሪክ ሂደት ሙቀት እንደሚከተለው ሊወከል ይችላል፡
Q=z / 2nRT.
እዚህ z የነፃነት ዲግሪዎች ብዛት ነው፣ይህም የሚወሰነው ጋዝ በሚፈጥሩት ሞለኪውሎች ፖሊቶሚክ ተፈጥሮ ነው። ለሞናቶሚክ ጋዝ፣ z=3፣ ለዲያቶሚክ ጋዝ - 5፣ እና ለትሪአቶሚክ እና ሌሎችም - 6. እዚህ፣ በነፃነት ደረጃዎች፣ የትርጉም እና የማዞሪያ ዲግሪዎች ማለታችን ነው።
የጋዝ ስርዓትን የማሞቅ ብቃትን በ isochoric እና isobaric ሂደቶች ውስጥ ብናነፃፅር በመጀመሪያ ሁኔታ ከፍተኛውን ቅልጥፍና እናገኛለን ምክንያቱም በስርዓቱ ሁኔታ ውስጥ የኢሶባሪክ ለውጥ በሚኖርበት ጊዜ ጋዝ ይስፋፋል እና የሙቀት ግቤት ከፊሉ ስራ ለመስራት ይውላል።
አይሶባራዊ ሂደት
ከዚህ በላይ ይህ isochoric ሂደት መሆኑን በዝርዝር ገልፀናል። አሁን ስለ ሌሎች isoprocesses ጥቂት ቃላት እንበል። በ isobaric እንጀምር። በስሙ ላይ በመመስረት, በቋሚ ግፊት በክፍለ-ግዛቶች መካከል የስርዓቱ ሽግግር እንደሆነ ተረድቷል. ይህ ሂደት በጌይ-ሉሳክ ህግ እንደሚከተለው ተገልጿል፡
V / T=const.
እንደ ኢሶኮሬ፣ ቪ(ቲ) አይሶባር በግራፉ ላይ ቀጥ ያለ መስመርን ይወክላል።
ለየማንኛውም የ isobaric ሂደት ከቋሚ ግፊት ውጤት እና ከድምጽ ለውጥ ጋር እኩል ስለሆነ በጋዝ የተሰራውን ስራ ለማስላት ምቹ ነው።
Isothermal ሂደት
ይህ የስርዓቱ የሙቀት መጠን ቋሚ ሆኖ የሚቆይበት ሂደት ነው። እሱ በቦይል-ማሪዮት ሕግ ለትክክለኛ ጋዝ ይገለጻል። ይህ በሙከራ የተገኘ የመጀመሪያው የጋዝ ህግ (የ 17 ኛው ክፍለ ዘመን ሁለተኛ አጋማሽ) መሆኑን ለማወቅ ጉጉ ነው. የሂሳብ መግለጫው ይህን ይመስላል፡
PV=const.
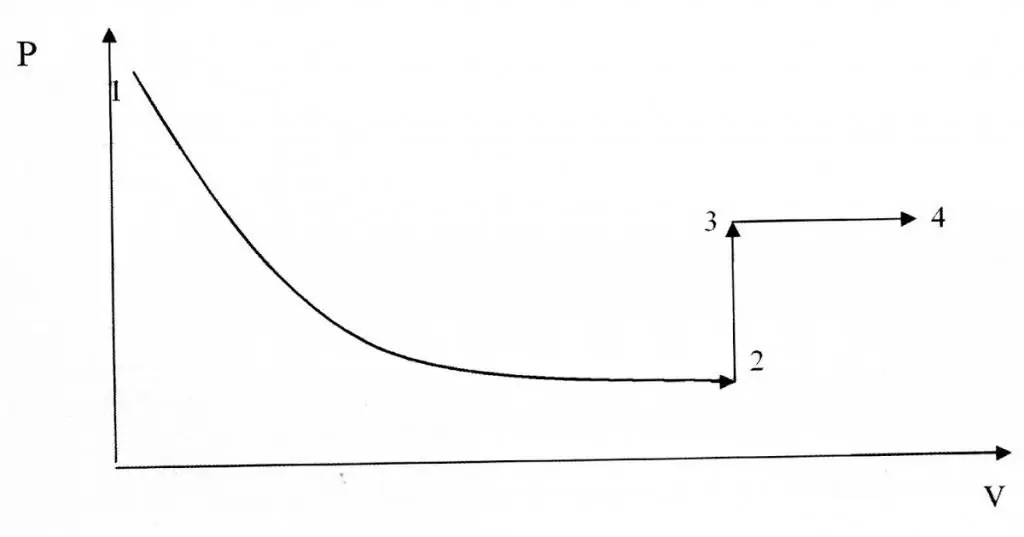
Isochoric እና isothermal ሂደቶች በስዕላዊ መግለጫቸው ይለያያሉ፣ምክንያቱም P(V) ተግባር ሃይፐርቦሊክ እንጂ መስመራዊ ግንኙነት አይደለም።
የችግር አፈታት ምሳሌ
በጽሁፉ ውስጥ የቀረቡትን የንድፈ ሃሳባዊ መረጃዎችን በማመልከቻው ተግባራዊ ችግር ለመፍታት እናጣምር። ንጹህ የጋዝ ናይትሮጅን በሲሊንደር ውስጥ በ 1 ከባቢ አየር ግፊት እና በ 25 ° ሴ የሙቀት መጠን ውስጥ እንደነበረ ይታወቃል. የጋዝ ሲሊንደር በማሞቅ እና በውስጡ ያለው ግፊት ከተለካ በኋላ 1.5 ከባቢ አየር ሆኗል. ከማሞቅ በኋላ በሲሊንደሩ ውስጥ ያለው የጋዝ ሙቀት ምን ያህል ነው? በ ፊኛ ውስጥ 4 ሞል ናይትሮጅን ከነበረ የጋዙ ውስጣዊ ሃይል በምን መጠን ተለወጠ።
የመጀመሪያውን ጥያቄ ለመመለስ የሚከተለውን አገላለጽ እንጠቀማለን፡
P1 / ቲ1=P2 / ቲ 2.
ከምንገኝበት፡
T2=P2 / P1 ቲ 1.
በዚህ አገላለጽ ግፊት በዘፈቀደ አሃዶች ሊተካ ይችላል።መለኪያዎች, እየቀነሱ ስለሆኑ, እና የሙቀት መጠኑ በኬልቪን ውስጥ ብቻ ነው. ይህን ከተናገረ በኋላ፡ እናገኛለን
T2=1.5 /1298.15=447.224 ኪ.
በዲግሪ ሴልሺየስ የሚሰላው የሙቀት መጠን 174°C ነው።
የናይትሮጅን ሞለኪውል ዲያቶሚክ ስለሆነ በማሞቅ ጊዜ የውስጣዊ ሃይሉ ለውጥ እንደሚከተለው ሊወሰን ይችላል፡
ΔU=5/2nRΔT.
በዚህ አገላለጽ የታወቁትን እሴቶች በመተካት ለችግሩ ሁለተኛ ጥያቄ መልሱን እናገኛለን ΔU=+12.4 kJ.






