በፊዚክስ ውስጥ በቴርሞዳይናሚክስ ሲስተም ጥናት ውስጥ ካሉት አስፈላጊ ጥያቄዎች አንዱ ይህ ስርዓት አንዳንድ ጠቃሚ ስራዎችን ማከናወን ይችላል የሚለው ነው። ከሥራ ጽንሰ-ሐሳብ ጋር በቅርበት የሚዛመደው የውስጣዊ ጉልበት ጽንሰ-ሐሳብ ነው. በዚህ ጽሁፍ ውስጥ የአንድ ተስማሚ ጋዝ ውስጣዊ ሃይል ምን እንደሆነ እንመለከታለን እና እሱን ለማስላት ቀመሮችን እንሰጣለን.
ጥሩ ጋዝ
ስለ ጋዝ፣ እንደ የመደመር ሁኔታ፣ በእሱ ላይ ምንም አይነት የመለጠጥ ሃይል የሌለው እና በውጤቱም መጠኑን እና ቅርፅን የማይይዝ፣ እያንዳንዱ የትምህርት ቤት ልጅ ያውቃል። ለብዙዎች ተስማሚ የሆነ ጋዝ ጽንሰ-ሐሳብ ለመረዳት የማይቻል እና ግልጽ ያልሆነ ነው. እናብራራው።
ጥሩ ጋዝ የሚከተሉትን ሁለት አስፈላጊ ሁኔታዎችን የሚያሟላ ማንኛውም ጋዝ ነው፡
- የሚሠሩት ቅንጣቶች ምንም መጠን የላቸውም። መጠናቸው አላቸው ነገርግን በመካከላቸው ካለው ርቀቶች ጋር ሲወዳደር በጣም ትንሽ ስለሆነ በሁሉም የሂሳብ ስሌቶች ችላ ሊባል ይችላል።
- ክንጣዎች የቫን ደር ዋልስ ሃይሎችን ወይም ሃይሎችን በመጠቀም አይገናኙም።ሌላ ተፈጥሮ. እንደ እውነቱ ከሆነ በሁሉም እውነተኛ ጋዞች ውስጥ እንዲህ ዓይነቱ መስተጋብር አለ, ነገር ግን ጉልበቱ ከኪነቲክ ቅንጣቶች አማካኝ ኃይል ጋር ሲነጻጸር እዚህ ግባ የሚባል አይደለም.
የተገለጹት ሁኔታዎች በሁሉም እውነተኛ ጋዞች ረክተዋል ፣የሙቀት መጠኑ ከ 300 ኪ.ሜ በላይ ነው ፣ እና ግፊቶቹ ከአንድ ከባቢ አየር አይበልጡም። ለከፍተኛ ግፊቶች እና ዝቅተኛ የሙቀት መጠኖች ከተገቢው ባህሪ የጋዞች መዛባትን ይመለከታል። በዚህ ሁኔታ አንድ ሰው ስለ እውነተኛ ጋዞች ይናገራል. በቫን ደር ዋልስ እኩልታ ተገልጸዋል።
የሀሳብ ጋዝ የውስጥ ሃይል ጽንሰ-ሀሳብ
በትርጓሜው መሰረት የአንድ ስርአት ውስጣዊ ሃይል በዚህ ስርአት ውስጥ የተካተቱት የኪነቲክ እና እምቅ ሃይሎች ድምር ነው። ይህ ጽንሰ-ሐሳብ ተስማሚ በሆነ ጋዝ ላይ ከተተገበረ, እምቅ አካል መጣል አለበት. በእርግጥም, ተስማሚ ጋዝ ቅንጣቶች እርስ በርስ መስተጋብር ስለማይፈጥሩ, በፍፁም ቫክዩም ውስጥ በነፃነት እንደሚንቀሳቀሱ ሊቆጠሩ ይችላሉ. በጥናት ላይ ካለው ስርዓት አንድ ቅንጣትን ለማውጣት እነዚህ ሃይሎች ስለሌሉ ከውስጥ የትብብር ሃይሎች ጋር የሚቃረን ስራ መስራት አያስፈልግም።
በመሆኑም የሃሳቡ ጋዝ ውስጣዊ ሃይል ሁል ጊዜ ከኪነቲክ ሃይሉ ጋር ይገጣጠማል። የኋለኛው ደግሞ በተራው ፣ በልዩ ሁኔታ የሚወሰነው በስርአቱ ቅንጣቶች ውስጥ ባለው የሞላር ብዛት ፣ ቁጥራቸው ፣ እንዲሁም የትርጉም እና የማሽከርከር እንቅስቃሴ አማካይ ፍጥነት ነው። የእንቅስቃሴው ፍጥነት በሙቀት መጠን ይወሰናል. የሙቀት መጠን መጨመር የውስጣዊ ጉልበት መጨመርን ያመጣል, እና በተቃራኒው.
ፎርሙላ ለየውስጥ ጉልበት
የሃሳባዊ ጋዝ ስርዓትን ውስጣዊ ሃይል በ U በሚለው ፊደል አመልክት ። በቴርሞዳይናሚክስ መሰረት ፣ እሱ በስርዓቱ enthalpy H እና የግፊት እና የመጠን ምርት መካከል ያለው ልዩነት ተብሎ ይገለጻል ፣ ይህ ማለት:
U=H - pV.
ከላይ ባለው አንቀጽ የU ዋጋ ከጠቅላላ የኪነቲክ ኢነርጂ Ekየሁሉም የጋዝ ቅንጣቶች፡
ጋር እንደሚዛመድ ደርሰንበታል።
U=ኢk።
ከስታቲስቲካዊ መካኒኮች፣ በሞለኪውላር ኪነቲክ ቲዎሪ (MKT) ሃሳባዊ ጋዝ ማዕቀፍ ውስጥ፣ የአንድ ቅንጣት አማካኝ የኪነቲክ ሃይል Ek1 ከ የሚከተለው እሴት፡
ኢk1=z/2kBT.
እዚህ kB እና ቲ - ቦልትዝማን ቋሚ እና የሙቀት መጠን፣ z - የነፃነት ዲግሪዎች ብዛት። የስርዓቱ አጠቃላይ የኪነቲክ ሃይል ኢk በስርዓቱ ውስጥ ባሉት ቅንጣቶች N ቁጥር፡ በማባዛት ማግኘት ይቻላል።
ኢk=Nኢk1=z/2NkBT.
በመሆኑም በአጠቃላይ በፍፁም የሙቀት መጠን እና በተዘጋ ስርዓት ውስጥ ካሉት የንጥረ ነገሮች ብዛት አንፃር የተፃፈ የሃሳባዊ ጋዝ ውስጣዊ ሃይል ቀመርን አግኝተናል፡
U=z/2NkBT.
Monatomic and polyatomic gas
በአንቀጹ ቀደም ባለው አንቀጽ ላይ የተፃፈው የዩ ቀመር ለተግባራዊ አጠቃቀሙ የማይመች ነው፣የቁጥር N ን ብዛት ለመወሰን አስቸጋሪ ስለሆነ። ነገር ግን፣ የንጥረ ነገሩን መጠን ትርጉም ከግምት ውስጥ የምናስገባ ከሆነ n፣ እንግዲያውስ ይህ አገላለጽ ይበልጥ ምቹ በሆነ መልኩ እንደገና ሊፃፍ ይችላል፡
n=N/NA; R=NAkB=8, 314 J/(molK)፤
U=z/2nR T.
የነጻነት ዲግሪዎች ብዛት በጋዝ በሚፈጥሩት ቅንጣቶች ጂኦሜትሪ ይወሰናል። ስለዚህ፣ ለሞኖአቶሚክ ጋዝ፣ z=3፣ አቶም ራሱን ችሎ የሚንቀሳቀስ በሦስት የጠፈር አቅጣጫዎች ብቻ ስለሆነ። ጋዝ ዲያቶሚክ ከሆነ, ከዚያም z=5, ሁለት ተጨማሪ የማዞሪያ የነጻነት ዲግሪዎች ወደ ሶስት የትርጉም ደረጃዎች ነፃነት ስለሚጨመሩ. በመጨረሻም, ለማንኛውም ሌላ ፖሊቶሚክ ጋዝ, z=6 (3 የትርጉም እና 3 የማዞሪያ ዲግሪዎች). ይህንን ከግምት ውስጥ በማስገባት ለሞናቶሚክ ፣ ዲያቶሚክ እና ፖሊአቶሚክ ተስማሚ ጋዝ ውስጣዊ ኃይል ቀመሮችን በሚከተለው መልክ መጻፍ እንችላለን-
U1=3/2nRT፤
U2=5/2nRT፤
U≧3=3nRT.
የውስጥ ሃይልን ለመወሰን የተግባር ምሳሌ
አንድ 100-ሊትር ሲሊንደር በ3 ከባቢ አየር ግፊት ንጹህ ሃይድሮጂን ይይዛል። በተሰጡት ቅድመ ሁኔታዎች ሃይድሮጂን ተስማሚ ጋዝ ነው ብለን ከወሰድን የውስጥ ሃይሉ ምን እንደሆነ መወሰን ያስፈልጋል።

ከላይ ያሉት የ U ቀመሮች የንጥረ ነገር መጠን እና የጋዝ ሙቀትን ይይዛሉ። በችግሩ ሁኔታ ውስጥ ስለእነዚህ መጠኖች ምንም አልተነገረም. ችግሩን ለመፍታት ሁለንተናዊውን የ Clapeyron-Mendeleev እኩልታ ማስታወስ አስፈላጊ ነው. በሥዕሉ ላይ የሚታየውን መልክ አለው።
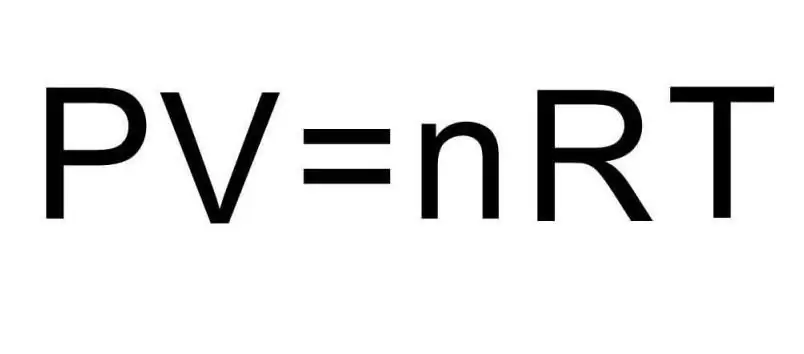
ሃይድሮጂን ኤች2 ዲያቶሚክ ሞለኪውል ስለሆነ የውስጥ ሃይል ቀመር፡
UH2=5/2nRT.
ሁለቱንም አባባሎች በማነፃፀር ለችግሩ መፍትሄ የመጨረሻው ቀመር ላይ ደርሰናል፡
UH2=5/2PV.
የግፊት እና መጠን ክፍሎችን ከሁኔታዎች ወደ SI የክፍል ክፍሎች ለመቀየር ይቀራል፣በቀመር ውስጥ ያሉትን ተዛማጅ እሴቶች በUH2እና ያግኙ። መልስ፡- UH2 ≈ 76 ኪጁ።






