የፊዚክስ የትርጓሜ እውቀት የተለያዩ የአካል ችግሮችን በተሳካ ሁኔታ ለመፍታት ቁልፍ ምክንያት ነው። በጽሁፉ ውስጥ፣ አይዞባሪክ፣ ኢሶኮሪክ፣ ኢሶተርማል እና አድያባቲክ ሂደቶች ለተገቢው የጋዝ ስርዓት ምን ማለት እንደሆነ እንመለከታለን።
ጥሩ ጋዝ እና ሒሳቡ
ወደ አይዞባሪክ፣ አይዞሆሪክ እና ኢሶተርማል ሂደቶች ገለጻ ከመቀጠልዎ በፊት ጥሩ ጋዝ ምን እንደሆነ እናስብ። በዚህ የፊዚክስ ፍቺ መሠረት በሁሉም አቅጣጫዎች በከፍተኛ ፍጥነት የሚንቀሳቀሱ እጅግ በጣም ብዙ ልኬቶች እና የማይገናኙ ቅንጣቶችን ያቀፈ ስርዓትን ያስባሉ። እንደውም የምንናገረው ስለ ቁስ አካል ጋስ አግሬጌት ሁኔታ ነው፣ በአተሞች እና ሞለኪውሎች መካከል ያለው ርቀት ከስፋታቸው እጅግ የላቀ እና የንጥረ ነገሮች መስተጋብር ሃይል ከኪነቲክ ኢነርጂ ጋር ሲነፃፀር በትናንሽነቱ ምክንያት ችላ ስለሚል ነው።
የጥሩ ጋዝ ሁኔታ የቴርሞዳይናሚክስ መለኪያዎች አጠቃላይ ነው። ዋናዎቹ የሙቀት መጠን, መጠን እና ግፊት ናቸው. በቅደም ተከተል በ T፣ V እና P ፊደሎች እንጠቁማቸው። በ 19 ኛው ክፍለ ዘመን በ 30 ዎቹ ውስጥክላፔሮን (የፈረንሣይ ሳይንቲስት) በመጀመሪያ በአንድ እኩልነት ውስጥ የተጠቆሙትን ቴርሞዳይናሚክስ መለኪያዎችን የሚያጣምር ቀመር ፃፈ። ይህን ይመስላል፡
PV=nRT፣
N እና R የቁሳቁሶች ብዛት እና የጋዝ ቋሚው በቅደም ተከተል ናቸው።
በጋዞች ውስጥ ያሉት isoprocesses ምንድን ናቸው?
ብዙዎች እንዳስተዋሉት፣ isobaric፣ isochoric እና isothermal ሂደቶች በስማቸው ተመሳሳይ የ"iso" ቅድመ ቅጥያ ይጠቀማሉ። በጠቅላላው ሂደት ውስጥ የአንድ ቴርሞዳይናሚክስ መለኪያ እኩልነት ማለት ሲሆን የተቀሩት መለኪያዎች ይለወጣሉ. ለምሳሌ የኢሶተርማል ሂደት እንደሚያመለክተው በውጤቱም የስርዓቱ ፍፁም የሙቀት መጠን ቋሚ ሆኖ ሲቆይ የኢሶኮሪክ ሂደት ግን ቋሚ መጠን ያሳያል።
Isoprocesses ለማጥናት ምቹ ናቸው፣ ምክንያቱም አንደኛውን ቴርሞዳይናሚክስ መለኪያዎች ማስተካከል አጠቃላይ የጋዝ ሁኔታን እኩልነት ወደ ቀላል ያደርገዋል። ለእነዚህ ሁሉ isoprocesses የጋዝ ህጎች በሙከራ የተገኙ መሆናቸውን ልብ ሊባል የሚገባው ጉዳይ ነው። የእነሱ ትንተና ክላፔሮን የተቀነሰውን ሁለንተናዊ እኩልታ እንዲያገኝ አስችሎታል።
ኢሶባሪክ፣ አይዞሆሪክ እና isothermal ሂደቶች
የመጀመሪያው ህግ ለአይኦተርማል ሂደት በተመጣጣኝ ጋዝ ውስጥ ተገኝቷል። አሁን የቦይል-ማሪዮት ሕግ ይባላል። ቲ የማይለወጥ በመሆኑ የስቴት እኩልነት እኩልነትን ያሳያል፡
PV=const.
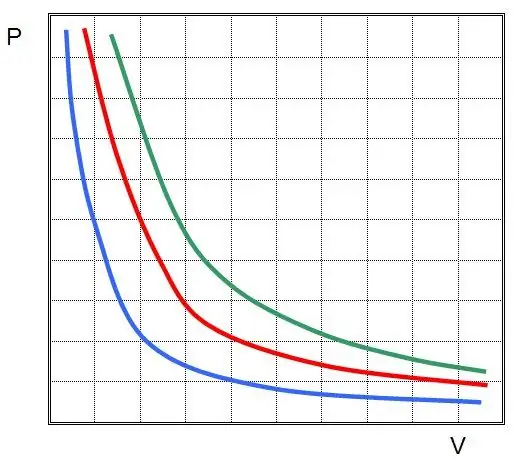
በሌላ አነጋገር በሲስተሙ ውስጥ ያለው ማንኛውም የግፊት ለውጥ የጋዝ የሙቀት መጠኑ ቋሚ ሆኖ የሚቆይ ከሆነ በድምጽ መጠኑ ላይ ወደ ተቃራኒው ተመጣጣኝ ለውጥ ያመራል። የተግባሩ ግራፍ P (V) ነው።ሃይፐርቦሌ።
Isobaric ሂደት - ይህ የስርዓቱ ሁኔታ ለውጥ ነው, ግፊቱ ቋሚ ሆኖ ይቆያል. የP ዋጋን በክላፔይሮን እኩል ካስተካከልን፣ የሚከተለውን ህግ እናገኛለን፡
V/T=const.
ይህ እኩልነት በ18ኛው ክፍለ ዘመን መገባደጃ ላይ የተቀበለውን የፈረንሳዊውን የፊዚክስ ሊቅ ዣክ ቻርልስ ስም ይዟል። ኢሶባር (የ V (T) ተግባር ግራፊክ ውክልና) ቀጥ ያለ መስመር ይመስላል። በስርዓቱ ውስጥ ያለው ግፊት በጨመረ ቁጥር ይህ መስመር በፍጥነት ይጨምራል።
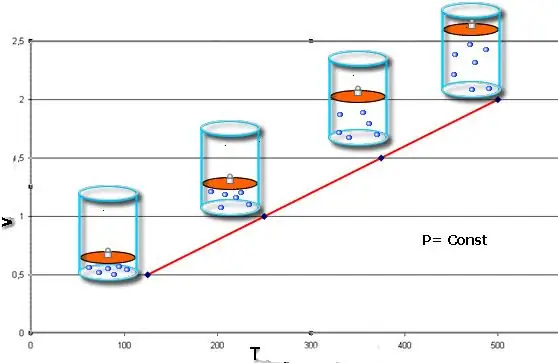
ጋዙ በፒስተን ስር ከተሞቀ የኢሶባሪክ ሂደትን ለመተግበር ቀላል ነው። የኋለኞቹ ሞለኪውሎች ፍጥነታቸውን (የኪነቲክ ሃይል) ይጨምራሉ, በፒስተን ላይ ከፍተኛ ጫና ይፈጥራሉ, ይህም ወደ ጋዝ መስፋፋት እና የ P.
ቋሚ እሴት ይጠብቃል.
በመጨረሻ፣ ሶስተኛው isoprocess isochoric ነው። በቋሚ ድምጽ ይሰራል. ከግዛቱ እኩልነት ተጓዳኝ እኩልነትን እናገኛለን፡
P/T=const.
በፊዚክስ ሊቃውንት ዘንድ የግይ-ሉሳክ ህግ በመባል ይታወቃል። በግፊት እና በፍፁም የሙቀት መጠን መካከል ያለው ቀጥተኛ ተመጣጣኝነት የኢሶኮሪክ ሂደት ግራፍ፣ ልክ እንደ አይዞባሪክ ግራፍ፣ አወንታዊ ተዳፋት ያለው ቀጥተኛ መስመር መሆኑን ያሳያል።
ሁሉም isoprocesses የተዘጉ ሲስተሞች ማለትም የ n ዋጋ በሂደታቸው እንደተጠበቀ መረዳት አስፈላጊ ነው።
አዲያባቲክ ሂደት
ይህ ሂደት የ"iso" ምድብ አይደለም፣ ምክንያቱም ሦስቱም የቴርሞዳይናሚክስ መለኪያዎች በሚያልፍበት ጊዜ ስለሚለዋወጡ። adiabaticከአካባቢው ጋር ሙቀትን የማይለዋወጥበት በሁለት የስርዓቱ ግዛቶች መካከል የሚደረግ ሽግግር ተብሎ ይጠራል. ስለዚህ የስርአቱ መስፋፋት የሚከናወነው በውስጣዊው የኢነርጂ ክምችቶች ምክንያት ነው, ይህም ከፍተኛ የሆነ የግፊት መቀነስ እና በውስጡ ያለው ፍጹም የሙቀት መጠን እንዲኖር ያደርጋል.
አድያባቲክ ለሃሳባዊ ጋዝ ሂደት የሚገለፀው በፖይሰን እኩልታዎች ነው። ከመካከላቸው አንዱ ከታች ይታያል፡
PVγ=const፣
የት γ የሙቀት አቅም ጥምርታ በቋሚ ግፊት እና በቋሚ መጠን።
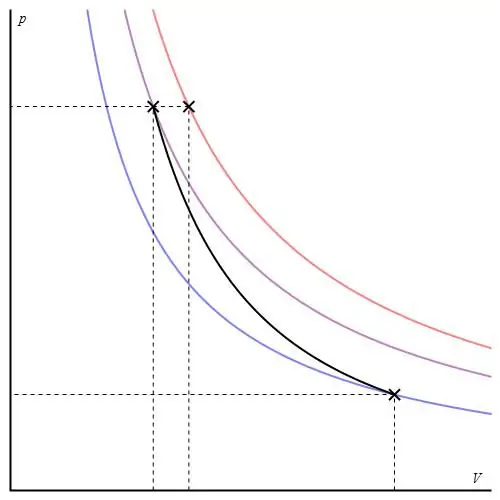
አዲያባቲክ ግራፍ ከአይዞሆሪክ ሂደት ግራፍ እና ከአይዞባሪክ ግራፍ ይለያል፣ነገር ግን ከሃይፐርቦላ (ኢሶተርም) ጋር ተመሳሳይ ነው። በP-V axes ውስጥ ያለው adiabat ከአይዞተርም የበለጠ ጠንከር ያለ ባህሪ አለው።






