Molecular-kinetic theory የስርዓቱን ጥቃቅን ባህሪ በመተንተን እና የስታቲስቲክስ ሜካኒክስ ዘዴዎችን በመጠቀም የቴርሞዳይናሚክ ስርዓትን አስፈላጊ ማክሮስኮፒ ባህሪያትን ለማግኘት ያስችላል። ከስርአቱ የሙቀት መጠን ጋር የተያያዘው ከአጉሊ መነጽር ባህሪያት አንዱ የጋዝ ሞለኪውሎች አማካኝ ካሬ ፍጥነት ነው. ለእሱ ቀመሩን ሰጥተን በጽሁፉ ውስጥ እንቆጥረዋለን።
ጥሩ ጋዝ
የጋዝ ሞለኪውሎች ኳድራቲክ አማካኝ ፍጥነት ቀመር በተለይ ለሀሳቡ ጋዝ እንደሚሰጥ ወዲያውኑ እናስተውላለን። በእሱ ስር ፣ በፊዚክስ ውስጥ ፣ ቅንጣቶች (አተሞች ፣ ሞለኪውሎች) እርስ በእርሳቸው የማይገናኙበት (የእነሱ የኪነቲክ ሃይል በብዙ የክብደት ትዕዛዞች መስተጋብር ከሚችለው ኃይል በላይ) እና ልኬቶች የሉትም ፣ በፊዚክስ ውስጥ እንደዚህ ያለ ብዙ ቅንጣት ስርዓት ይቆጠራል። ማለትም፣ ውሱን የሆነ ክብደት ያላቸው ነጥቦች ናቸው (በንጥሎች መካከል ያለው ርቀት ከትልቅነታቸው የሚበልጡ በርካታ የክብደት መጠኖች።መስመራዊ)።
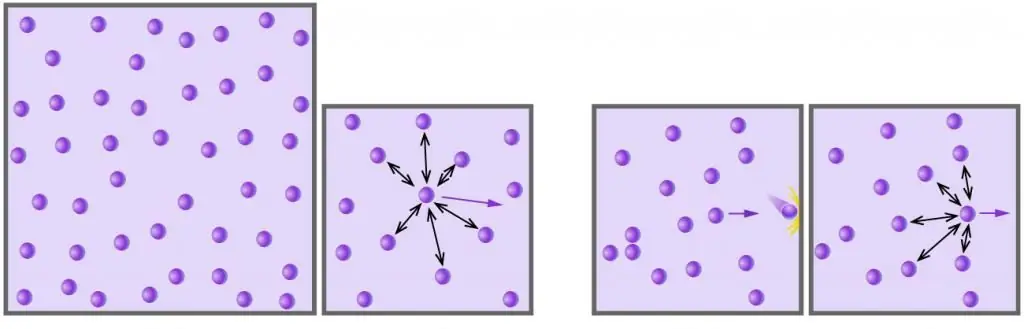
ከኬሚካል ገለልተኛ የሆኑ ሞለኪውሎች ወይም አቶሞችን ያቀፈ እና ዝቅተኛ ግፊት ያለው እና ከፍተኛ ሙቀት ያለው ማንኛውም ጋዝ ጥሩ ነው ተብሎ ሊወሰድ ይችላል። ለምሳሌ, አየር ተስማሚ ጋዝ ነው, ነገር ግን የውሃ ትነት እንደዚህ አይደለም (ጠንካራ የሃይድሮጂን ቦንዶች በውሃ ሞለኪውሎች መካከል ይሠራሉ).
Molecular Kinetic Theory (MKT)

በMKT ማዕቀፍ ውስጥ ጥሩ ጋዝ በማጥናት ለሁለት አስፈላጊ ሂደቶች ትኩረት መስጠት አለቦት፡
- ጋዝ ወደያዘው የመርከቧ ግድግዳዎች በማዛወር ጫና ይፈጥራል ይህም ሞለኪውሎች እና አተሞች ከነሱ ጋር የሚጋጩበት ጊዜ ነው። እንደዚህ ያሉ ግጭቶች ፍጹም የመለጠጥ ችሎታ አላቸው።
- ሞለኪውሎች እና የጋዝ አቶሞች በዘፈቀደ ወደ ሁሉም አቅጣጫዎች በተለያዩ ፍጥነቶች ይንቀሳቀሳሉ፣ ስርጭቱም የማክስዌል-ቦልትዝማንን ስታቲስቲክስ ያከብራል። በትንሽ መጠን እና በመካከላቸው ያለው ትልቅ ርቀት ምክንያት የመጋጨት እድሉ እጅግ በጣም ዝቅተኛ ነው።
የጋዝ ቅንጣቶች ግለሰባዊ ፍጥነቶች አንዳቸው ከሌላው በጣም የተለዩ ቢሆኑም በሲስተሙ ላይ ምንም ውጫዊ ተጽእኖዎች ከሌሉ የዚህ እሴት አማካኝ ዋጋ በጊዜ ሂደት ይቆያል። የጋዝ ሞለኪውሎች አማካኝ ካሬ ፍጥነት ቀመር የሚገኘው በኪነቲክ ሃይል እና በሙቀት መካከል ያለውን ግንኙነት ግምት ውስጥ በማስገባት ነው። ይህንን ጉዳይ በሚቀጥለው የአንቀጹ አንቀፅ ውስጥ እናስተናግዳለን።
የቀመርው አመጣጥ ተስማሚ የጋዝ ሞለኪውሎች ባለአራት አማካይ ፍጥነት
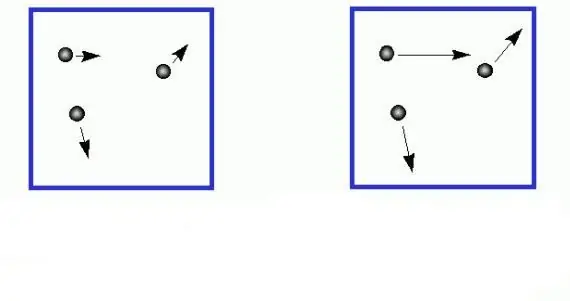
እያንዳንዱ ተማሪ ከአጠቃላይ የፊዚክስ ኮርስ የሚያውቀው የሰውነት የትርጉም እንቅስቃሴ ኪነቲክ ሃይል በጅምላ m በሚከተለው መልኩ ይሰላል፡
ኢk=mv2/2
ቁ የሆነ የመስመር ፍጥነት ነው። በሌላ በኩል፣ የአንድ ቅንጣት እንቅስቃሴ (kinetic energy) እንዲሁ ከፍፁም የሙቀት መጠን T አንፃር ሊታወቅ ይችላል፣ የልወጣ ፋክተር kB(የቦልዝማን ቋሚ) በመጠቀም። የእኛ ቦታ ባለ ሶስት አቅጣጫዊ ስለሆነ ኢk እንደሚከተለው ይሰላል፡
ኢk=3/2kBT.
ከሁለቱም እኩልነቶች ጋር እኩል የሆነ እና ቪን ከነሱ በመግለጽ የኳድራቲክ ሃሳባዊ ጋዝ አማካይ ፍጥነት ቀመርን እናገኛለን፡
mv2/2=3/2kBT=>
v=√(3kBT/m)።
በዚህ ቀመር m - የጋዝ ቅንጣት ብዛት ነው። እሴቱ ትንሽ ስለሆነ (≈ 10-27kg) ስለሆነ በተግባራዊ ስሌቶች ለመጠቀም ምቹ አይደለም። ይህንን ችግር ለማስቀረት፣ ሁለንተናዊ የጋዝ ቋሚውን R እና የሞላር ክብደት ኤም እናስታውስ።
kB=R/NA።
የኤም ዋጋ እንደሚከተለው ይገለጻል፡
M=mNA።
ሁለቱንም እኩልነት ከግምት ውስጥ በማስገባት ለሞለኪውሎች ሥር-አማካኝ-ካሬ ፍጥነት የሚከተለውን አገላለጽ እናገኛለን፡
v=√(3RT/M)።
በመሆኑም የጋዝ ቅንጣቶች አማካኝ የካሬ ፍጥነት ከካሬው ፍፁም የሙቀት መጠን ጋር ቀጥተኛ ተመጣጣኝ እና ከሞላር ክብደት ስኩዌር ስር በተገላቢጦሽ ነው።
የችግር አፈታት ምሳሌ
የምንተነፍሰው አየር 99% ናይትሮጅን እና ኦክሲጅን መሆኑን ሁሉም ሰው ያውቃል። በ15 o የሙቀት መጠን N2 እና O2 የሞለኪውሎች አማካኝ ፍጥነቶች ልዩነቶችን ማወቅ ያስፈልጋል። C.

ይህ ችግር በቅደም ተከተል ይፈታል። በመጀመሪያ የሙቀት መጠኑን ወደ ፍፁም አሃዶች እንተረጉማለን፡-
አለን
T=273, 15 + 15=288, 15 K.
አሁን እየታሰበበት ላለው ለእያንዳንዱ ሞለኪውል የሞላር ስብስቦችን ይፃፉ፡
MN2=0.028 ኪግ/ሞል፤
MO2=0.032 ኪግ/ሞል።
የሞላር ብዙኃን ዋጋዎች ትንሽ ስለሚለያዩ በተመሳሳይ የሙቀት መጠን አማካኝ ፍጥነታቸው እንዲሁ ቅርብ መሆን አለበት። ለ v ቀመሩን በመጠቀም ለናይትሮጅን እና ለኦክስጅን ሞለኪውሎች የሚከተሉትን እሴቶች እናገኛለን፡
v (N2)=√(38, 314288, 15/0, 028)=506.6 m/s;
v (O2)=√(38, 314288, 15/0, 032)=473.9 m/s.
የናይትሮጅን ሞለኪውሎች ከኦክስጅን ሞለኪውሎች ትንሽ ቀለለ ስለሆኑ በፍጥነት ይንቀሳቀሳሉ። አማካይ የፍጥነት ልዩነት፡
ነው።
v (N2) - v (O2)=506.6 - 473.9=32.7 m/ s.
የተገኘው ዋጋ ከአማካይ የናይትሮጅን ሞለኪውሎች ፍጥነት 6.5% ብቻ ነው። በጋዞች ውስጥ ያሉ የሞለኪውሎች ከፍተኛ ፍጥነት በዝቅተኛ የሙቀት መጠንም ቢሆን ትኩረትን እናሳያለን።






